実験的トキソプラズマワクチンがどのように効くかを解明!
―宿主タンパク質 p62を標的とした新たなワクチンの開発に前進―
p62 Plays a Specific Role in Interferon-γ-Induced Presentation of a Toxoplasma Vacuolar Antigen
Cell Reports Available online 2 Oct 2015 論文
概要
p62と呼ばれる宿主分子が、病原性寄生虫「トキソプラズマ」の実験的不活化ワクチンの免疫的効果発揮に重要な役割を果たすことを発見しました。
背景
トキソプラズマはエイズや抗癌剤投与下にある免疫不全の大人で致死的な脳炎や肺炎を引き起こす病原体です。また、健康な妊婦が初感染すると胎児に垂直感染し流産や死産、さらには新生児がトキソプラズマに感染した状態で生まれ先天性疾患の原因ともなります。現在、ヒトで使用可能なトキソプラズマのワクチンは存在せず、マウスなと?の実験動物を用いて不活化ワクチン開発のための基礎研究か進んでいます。しかし、トキソプラズマ不活化ワクチンがどのようにして免疫的効果を発揮するのか、特にワクチンを投与された側の体内でどのような免疫反応が最初に起きることが重要なのかについては、よく分かっていませんでした。
研究の成果
我々は、トキソプラズマの寄生胞にインターフェロン ガンマ依存的に蓄積する分子群の解析を以前から進めており、これまでにGBP な どの寄生胞破壊因子やRabGDIαを介した制御機構を報告してきました。その解析の中で、p62(およびユビキチン)と呼ばれる宿主分子群が寄生胞にインターフェロン ガンマ刺激依存的に蓄積 することも見出していました(図2A および図4)。インターフェロン ガンマ刺激によってトキソプラズマの殺傷に関与するGB P やRabGDIα などと異なり、p62 を欠損しても感染細胞内におけるトキソプラズマの数に変化はないことから(図2B)、GBP やRabGDIα などとは異なり、p62 は寄生胞に蓄積するにもかかわらずトキソプラズマの殺傷には関与しないことが明らかとなりました。
以前に先行研究により、寄生胞内に放出されたトキソプラズマ由来の抗原がキラーT 細胞の主要抗原になるということが明らかになったことから、我々はインターフェロン ガンマ刺激によってトキソプラズマ感染細胞を刺激した時のキラーT 細胞の活性化を検討しました。その結果、未刺激の感染細胞に比べて、インターフェロン ガンマに よって刺激した感染細胞では抗原特異的なキラーT 細胞の活性が劇的に上昇することを見出しました(図3A)。この感染細胞をインターフェロン ガンマ刺激した際に見られているキラーT 細胞の強い活性化は、p62 を欠損した感染細胞で は有意に低下し(図3B)、さらに個体レベルでも野生型マウスに比べて、p62 欠損マウスではトキソプラズマの不活化ワク チン投与による抗原特異的なキラーT 細胞の数が激減していました(図3C)。
以上の結果から、
① インターフェロン ガンマ刺激依存的に宿主タンパク質であるp62がトキソプラズマに蓄積すること
② トキソプラズマ感染細胞では、p62とインターフェロン ガンマ依存的にキラーT細胞活性化能が高まること
③ p62欠損マウス個体で、トキソプラズマ不活化ワクチン投与に対するキラーT細胞活性が著しく低下すること
が明らかになり、p62 はインターフェロン ガンマ刺激に依存してトキソプラズマの寄生胞に蓄積し、寄生胞内に放出さ れた抗原特異的にキラーT 細胞の活性化を担うという、これまでに報告されていないユニークな役割を持っていることが 明らかとなりました(図4)。
今後の期待
本研究で我々は、トキソプラズマ寄生胞放出タンパク質特異的なキラーT 細胞活性化における p62 のユニークな機能を発見しました。我々の発表とほぼ同時に独立して米国グループはヒトの細胞においてもイ ンターフェロン ガン マ刺激的にp62 がトキソプラズマ寄生胞に蓄積することを発見し、報告しており、今回 の我々の発見した研究成果は、マウスのみならずヒトにも当てはまることが十分に予想されます。ワクチン開発が進まず、我が国を含め半ば「無視された感染症(Neglected Infectious Diseases)」の状態となっているトキソプラズマ 症に対して、p62 を新たな標的としその機能を高める等によって新規の治療・予防戦略を提供できることが期待されます。
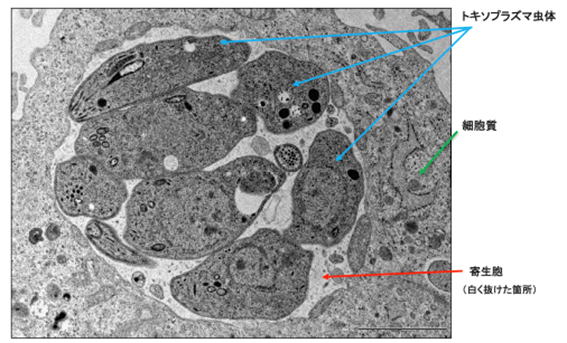
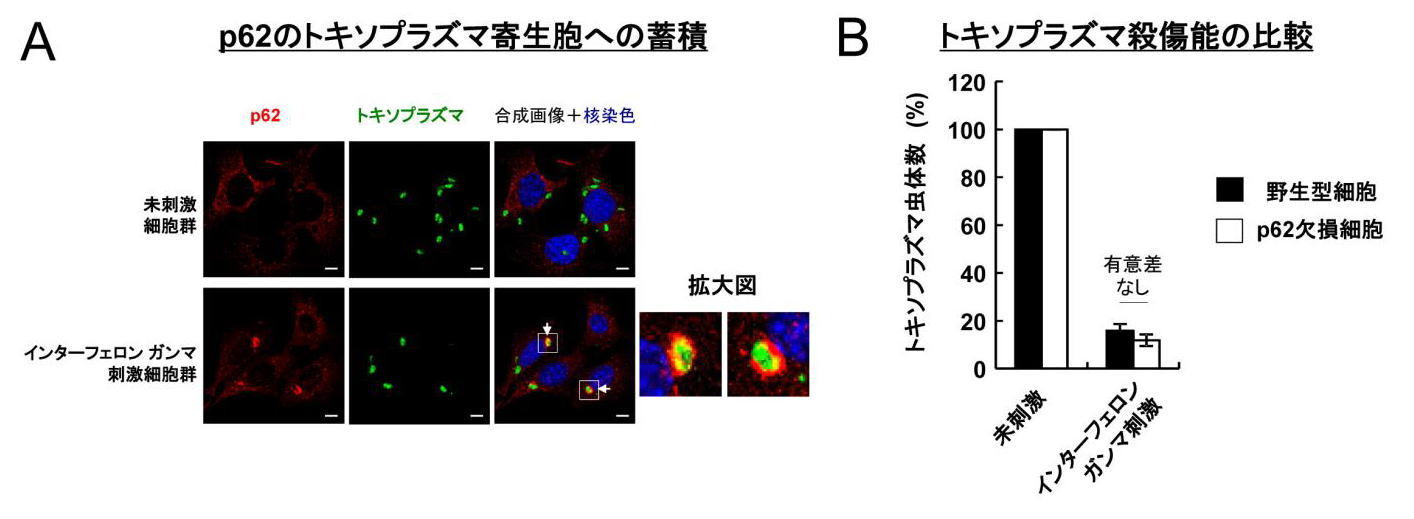
図2 p62 はインターフェロン ガンマ刺激依存的に寄生胞に蓄積するが、殺傷能には関係ない
(A) p62 (赤色)がトキソプラズマ(緑色)と共局在していることを示す顕微鏡写真。
(B) 野生型細胞とp62 欠損細胞を比較しても、インターフェロン ガンマ刺激後のトキソプラズマの虫体数は同様に低下している。すなわち、p62 欠損細胞においてもインターフェロン ガンマ依存的殺傷は起きていることを示している。
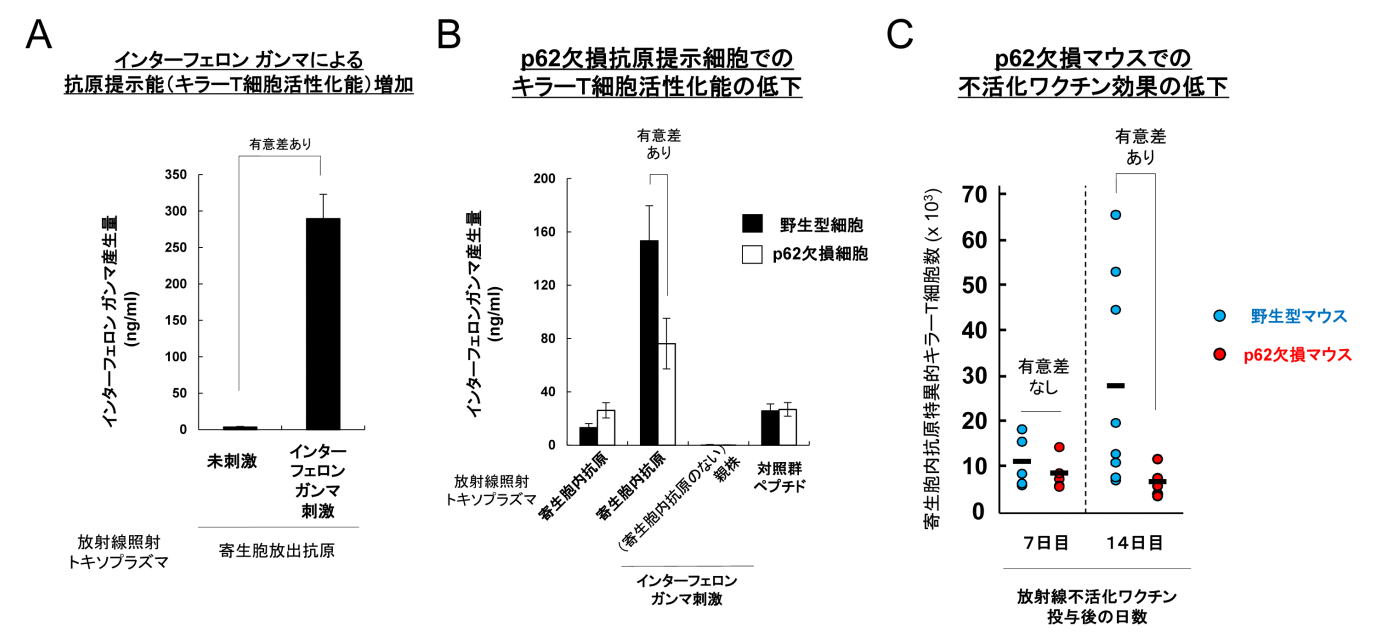
図3 p62 欠損細胞およびマウスでは寄生胞内抗原に対する特異的キラーT 細胞活性が低下する
(A) トキソプラズマに感染している抗原提示細胞である樹状細胞をインターフェロン ガンマで刺激すると、寄生胞内抗原特異的 キラーT 細胞に由来するインターフェロン ガンマの産生量(キラーT 細胞の活性化の指標)が爆発的に増加する。
(B) p62 欠損し た樹状細胞では(A)で見られたインターフェロン ガンマ刺激によるキラーT 細胞の活性化が、野生型樹状細胞に比べて低下している。
(C) 放射線不活化したトキソプラズマを投与後、14 日目の寄生胞内抗原特異的キラーT 細胞数がp62 欠損マウスではほとんど上昇していないことがわかる(すなわち、ワクチン効果が認められない)。
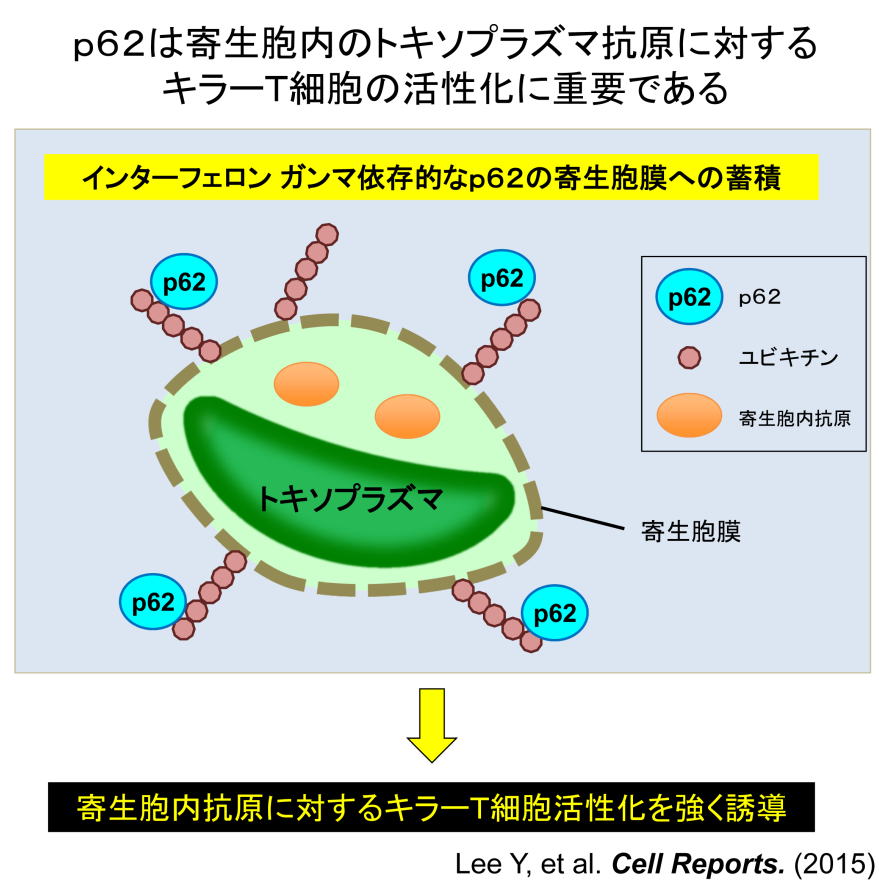
図4 p62 による寄生胞内抗原特異的 キラーT 細胞活性化機構
トキソプラズマが感染した細胞内では、インターフェロン ガンマ刺激依存的に、まずユビキチンが寄生胞に蓄積し、p62 が最終的に寄生胞膜に蓄積します。その結果、p62 依存的に寄生胞内に溜まったトキソプラズマのタンパク質が処理され、キラーT 細胞の抗原となっていると考えられます。
-
論文詳細12
詳細を見る -
論文詳細11
詳細を見る -
論文詳細10
詳細を見る -
論文詳細09
詳細を見る -
論文詳細08
ヒトの細胞で抗トキソプラズ免疫反応に重要な分子の同定
―宿主分子IDO1を中心とした宿主-病原体相互作用の解明―
Toxoplasma Effector TgIST Targets Host IDO1 to Antagonize the IFN-γ-Induced Anti-parasitic Response in Human Cells
詳細を見る -
論文詳細07
抗病原体分子をバランスよく配置して、免疫反応を効率化!
―GBP依存的な抗病原体免疫反応に重要な制御因子Gate-16の同定―
Essential role for GABARAP autophagy proteins in interferon-inducible GTPase-mediated host defense
詳細を見る -
論文詳細06
実験的トキソプラズマワクチンがどのように効くかを解明!
―宿主タンパク質 p62を標的とした新たなワクチンの開発に前進―
p62 Plays a Specific Role in Interferon-γ-Induced Presentation of a Toxoplasma Vacuolar Antigen
詳細を見る -
論文詳細05
世界初!寄生虫「トキソプラズマ」に対する免疫反応が大幅アップ!
―抗トキソプラズマ免疫反応のブレーキ役を果たす分子の同定―
RabGDIα is a negative regulator of interferon-γ-inducible GTPase-dependent cell-autonomous immunity to Toxoplasma gondii
詳細を見る -
論文詳細04
寄生虫「トキソプラズマ」は、どのように宿主の身体を乗っ取るか?
―高病原性因子 高病原性因子 GRA6「トロイの木馬」現象を引き起こす ―
Selective and strain-specific NFAT4 activation by the Toxoplasma gondii polymorphic dense granule protein GRA6.
詳細を見る -
論文詳細03
インターフェロン-ガンマ依存的な抗トキソプラズマ応答におけるオートファジー蛋白質の役割
Role of Mouse and Human Autophagy Proteins in IFN-γ-Induced Cell-Autonomous Responses against Toxoplasma gondii.
詳細を見る -
論文詳細02
CREBHによるスルピリンの副作用誘導機構
CREBHはスルピリンによって誘導される致死的ショックの重症度を決定する
CREBH Determines the Severity of Sulpyrine-induced Fatal Shock
詳細を見る -
論文詳細01
トキソプラズマ症の発病を防ぐ最重要宿主防御因子GBPの同定
インターフェロン誘導性タンパクGBPは寄生虫「トキソプラズマ」を破壊する
A Cluster of Interferon-γ-Inducible p65 GTPases Plays a Critical Role in Host Defense against Toxoplasma gondii
詳細を見る